


启迪专精特新|恒瑞源正靶向HPV18阳性实体瘤TCR-T研究成果发表于Nature Communications打印
发布时间:2024-03-19来源:药融圈公众号

▲ 研究成果发表于Nature Communications杂志
研究背景
宫颈癌(Cervical Cancer)是妇科常见的恶性肿瘤之一,发病率在女性恶性肿瘤中居第四位,目前国内外对于二线化疗失败的转移或复发性宫颈癌患者尚无可推荐的治疗方案。研究证实,95%以上的宫颈癌均与HPV(人乳头瘤病毒)相关,其中以16型和18型最为常见。此外,HPV感染还会导致多种头颈癌和肛门生殖器肿瘤。HPV感染后癌变的肿瘤细胞中会持续性高表达E7病毒蛋白,此蛋白在正常组织中不表达,是TCR-T等靶向治疗的优良靶点。
研究结果
本研究中,科研团队基于TCR逆向基因工程(Reverse Genetic Engineering of TCR,ReGET)平台技术,成功地从一位早期多抗原自体免疫细胞治疗(MASCT)获益患者体内克隆到靶向HPV18 E7肿瘤抗原的TCR分子(10F04 TCR)。该患者在2011年被诊断为HPV阳性晚期转移性宫颈鳞状细胞癌,经手术、化疗、放疗等常规治疗后复发。患者于2014年起,经过多疗程MASCT治疗后肿瘤逐渐消退并获得长期缓解,截至目前已无瘤生存超过九年。该患者体内针对HPV18 E7等多种肿瘤抗原特异性T细胞的长期存在是该患者临床获益的可能原因。
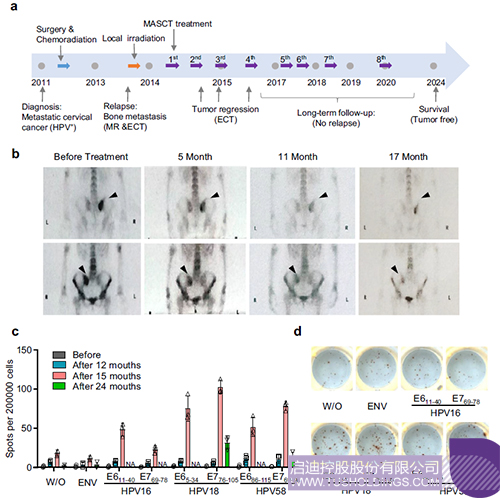
▲ MASCT免疫获益患者治疗概况及免疫相应
研究结果证实,10F04 TCR特异性识别中国人群高频的HLA-II分子HLA-DRB1*09:01递逞的HPV18 E7抗原肽,在体外和小鼠模型中均展现了强大的抗肿瘤活性。结果显示,10F04 TCR可同时介导CD4+和CD8+T细胞中实现对抗原阳性肿瘤细胞的识别和直接杀伤,并释放IFNγ, TNFα, IL2, Granzyme B等抗肿瘤细胞因子,进一步诱导肿瘤细胞凋亡并促进TCR-T细胞的扩增。同时,激活的TCR-T细胞分泌的IFNγ细胞因子也能诱导肿瘤表面HLA分子的表达上调,使其对TCR-T的识别更加敏感。近年来,越来越多的临床研究结果表明,CD4+肿瘤识别T细胞在肿瘤治疗中起到关键性的作用,通过直接杀伤,辅助CD8+T细胞的杀伤和长期存续,以及分泌细胞因子等途径调动DC,巨噬细胞等固有免疫系统实现针对肿瘤的抗肿瘤作用。本研究报道的10F04 TCR分子可实现CD4+和CD8+T细胞的同时激活并能分泌多种细胞因子;同时,本研究也对人类蛋白质组和主要HLA分子进行了交叉识别验证,未发现10F04TCR任何脱靶风险。
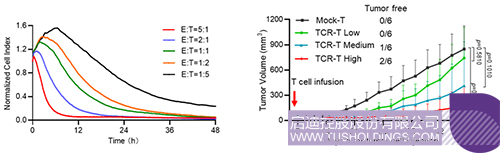
▲ 10F04 TCR-T细胞临床前药效
后续进展
目前,HRYZ-T101产品已获得CDE批准用于HPV18阳性实体瘤的治疗,I期注册临床试验已完成首例患者回输。
参考文献
Long, J. et al. HLA-class II restricted TCR targeting human papillomavirus type 18 E7 induces solid tumor remission in mice. Nature Communications 15, 2271 (2024).
关于TCR
T 细胞受体 (T cell receptor, TCR)分子可以同时识别细胞膜表面和细胞内几乎所有肿瘤细胞抗原,与嵌合抗原受体(CAR)分子相比在实体瘤治疗方面具有更大的优势和潜力。2022年,Immunocore公司的全球首个TCR融合CD3抗体的蛋白药物(Tebentafusp)获FDA批准上市,用于治疗葡萄膜黑色素瘤。2024年8月,Adaptimmune Therapeutics公司的全球首款针对实体瘤的TCR-T细胞治疗产品(Afami-cel)也将获得美国FDA的上市申请(BLA)批准,用于治疗滑膜肉瘤。
关于恒瑞源正
启迪漕河泾科技园区企业——恒瑞源正生物科技有限公司是由江苏恒瑞医药集团及深圳源正细胞医疗技术有限公司于2015年合资创立的一家聚焦细胞基因治疗(CGT)的生物医药企业。公司专注于实体瘤免疫治疗,开发了基于肿瘤特异性T细胞受体(TCR)和多靶点自体免疫细胞(MASCT)等多个产品管线。其中,MASCT- I为全球首个获得IND批准的双重免疫细胞治疗产品,已进入II期临床阶段;通过公司自主研发的ReGET平台孵化的首个TCR-T产品HRYZ-T101也已经获得IND批准,进入了I期临床阶段。ReGET平台可以持续孵化基于亚洲人群HLA分型的全球首创的TCR分子,解决了TCR产品总是基于欧美人群HLA分型的“卡脖子”问题。公司最新布局的TCR融合蛋白产品进一步解决了细胞治疗“现货化”的问题,大大提高了药物的可及性,有望造福更多中国实体瘤患者。公司在主营业务拥有超过60项核心专利,并在中国,美国,欧盟,日本等多个国家和地区获得授权。















 京公网安备11010802024130号
京公网安备11010802024130号